Ген, представляющий собой участок молекулы ДНК, несет в себе информацию для синтеза полипептидной цепи с определенной аминокислотной последовательностью, однако ген не принимает непосредственного участия в синтезе белка.
ДНК гена служит матрицей для молекулы РНК, так называемой информационной РНК — и-РНК.
Существует несколько типов РНК в клетке, но для всех них характерными являются такие общие признаки:
1) в РНК входит сахар рибоза в отличие от дезоксирибозы ДНК;
2) РНК, подобно ДНК, состоит из комбинаций четырех нуклеотидов, но в ней тимин замещен урацилом.
В настоящее время принято считать, что цепочки биспирали ДНК неравнозначны: на одной из них зашифрована структура полипептида — она имеет как бы смысловое значение, а другая, комплементарная ей, представляет собой так называемую антисмысловую цепочку. Именно смысловая цепочка служит матрицей для синтеза одиночной цепи и-РНК.
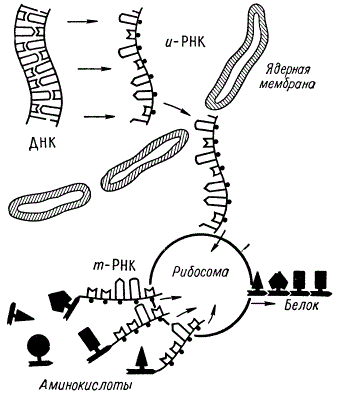
Схема синтеза белка в клетке
Под контролем фермента ДНК-зависимой РНК-полимеразы происходит как бы переписывание кода смысловой цепочки ДНК на и-РНК. Каждая молекула и-РНК существует в клетке несколько минут, после чего ген отпечатывает новые молекулы и-РНК. Молекула и-РНК поступает в цитоплазму, где на нее нанизываются рибосомы. Такой комплекс из и-РНК и нескольких рибосом носит название полисомы. Именно в полисомах происходит синтез белка.
Рибосомы представляют собой рибонуклеопротеиновые структуры, состоящие примерно наполовину из высокополимерной однонитчатой РНК (рибосомная РНК), а наполовину из белка. Каждая Рибосома движется по молекуле и-РНК, а тем временем на рибосоме растет полипептидная цепочка. Длина цепочки пропорциональна расстоянию, пройденному рибосомой от начала молекулы и-РНК. Число аминокислот в таком белковом фрагменте равно числу триплетов, которые успела «прочесть» рибосома.
Выстраивание аминокислотных остатков в соответствии с триплетами, или кодонами, и-РНК осуществляется на рибосомах при помощи еще одного типа молекул РНК, а именно транспортных РНК — т-РНК.
т-РНК низкополимерны, отдельная молекула состоит примерно из 70 нуклеотидов. В этой молекуле большинство водородных связей замкнуто, благодаря комплементарному взаимодействию оснований. Согласно одной из моделей строения т-РНК предполагается, что молекула представляет собой полинуклеотидный тяж, сложенный пополам и скрученный таким образом, что образовалась двойная спираль наподобие ДНК. В точке перегиба остаются три неспаренных нуклеотида, которые названы антикодоном. Именно триплет антикодона т-РНК благодаря наличию незамещенных водородных связей сможет взаимодействовать с находящимся на рибосоме триплетом кодона и-РНК. Другой конец молекулы т-РНК служит для соединения с аминокислотой. Каждый класс молекул т-РНК может соединяться только с одной аминокислотой; следовательно, количество разных молекул т-РНК должно быть не менее двадцати. Это взаимодействие контролируют высокоспецифичные активирующие ферменты аминоацил-т-РНК-синтетазы.
Итак, различные молекулы т-РНК приносят к рибосоме аминокислоты и располагают их соответственно последовательности триплетов и-РНК. Точность считывания генетической информации зависит не только от того, какие кодоны проходят через рибосому, но в значительной мере и от состояния самой рибосомы. Стоит изменить структуру рибосомы, присоединив к ней, например, молекулу антибиотика стрептомицина или повысив концентрацию ионов магния Mg++ в окружающей среде, как генетический код, отпечатанный в и-РНК, начинает считываться неправильно: рибосома «читает» с ошибками, часто включает «не те» аминокислоты в полипептидную цепь. Именно с этим и связано инактивирующее действие стрептомицина на бактериальные клетки. В ДНК гена, а следовательно, и в соответствующем участке т-РНК записана информация синтеза первичной структуры белка определенной аминокислотной последовательности.
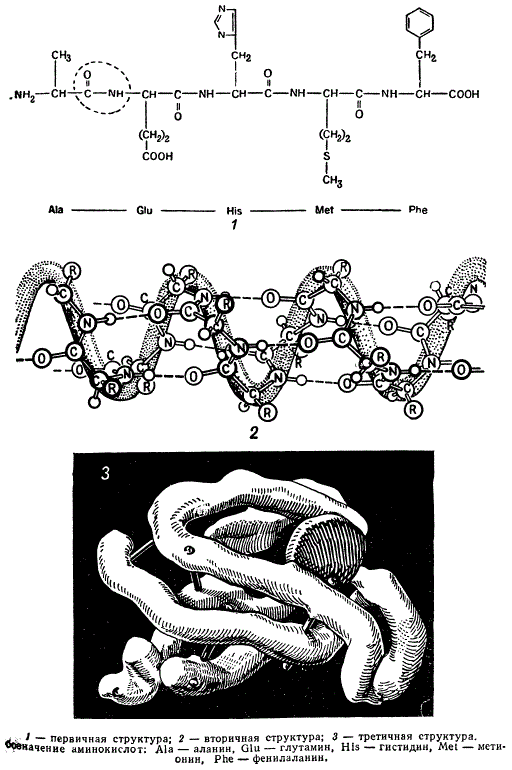
Строение белка
В белковой молекуле наряду с первичной структурой имеются структуры и более высоких порядков. Вторичная структура белка характеризуется образованием спиралей за счет водородных связей между соседними аминокислотными остатками. Полипептидная цепь, имеющая вторичную структуру, специфическим образом сворачивается и укладывается, образуя третичную структуру. Характер третичной структуры белка определяется наличием в полипептидной цепи пролиновых остатков, в точках нахождения которых образуются повороты цепи, наличием дисульфидных связей между разными участками цепи, а также взаимодействием полярных и неполярных аминокислотных остатков в молекуле. При этом молекула складывается таким образом, что полярные аминокислоты располагаются снаружи, а неполярные внутри образующейся глобулы. В ряде случаев такие свернутые белковые глобулы представляют собой готовые ферментные молекулы.
Известны ферменты с четвертичной структурой, когда две или более одинаковые молекулы, имеющие третичную структуру, объединяются, становясь субъединицами одной сложной ферментной молекулы. Следует различать два случая образования четвертичной структуры: 1) когда фермент построен из субъединиц, синтезированных под контролем одного гена, т. е. из идентичных субъединиц, и 2) когда фермент построен из субъединиц, синтезируемых под контролем разных генов, т. е. из неидентичных субъединиц. Таким ферментом, в молекуле которого можно различать и идентичные, и неидентичные субъединицы, является, например, гемоглобин. Молекула этого фермента состоит из двух α-цепей и двух β-цепей. α-цепи по отношению друг к другу — идентичные субъединицы, так же и β-цепи. В то же время α- и β-цепи между собой — неидентичные субъединицы.
Образование вторичной, третичной и четвертичной структур белковой молекулы в условиях данной клеточной среды или в одних и тех же условиях in vitro однозначно определяется первичной структурой молекулы.
Понимание основных моментов белкового синтеза позволило моделировать этот процесс в бесклеточных системах с использованием искусственно синтезированных и-РНК.
Подтверждение роли нуклеотидного кода в синтезе белка было получено в работах по синтезу полипептидов in vitro, когда впервые была сделана успешная попытка найти соответствие между триплетами, имеющими определенный состав нуклеотидов, и аминокислотами, включение которых в полипептидную цепочку контролируется данными триплетами. Этому способствовали два биохимических открытия: получение бесклеточных систем, в которых может идти синтез белка, и ферментативный синтез искусственных полирибонуклеотидов.
М. Ниренберг и Р. Маттэй впервые (1961 г.) показали, что искусственно синтезированные полирибонуклеотиды определенного состава, введенные в бесклеточную систему, содержащую рибосомы, полный набор аминокислот и некоторые ферменты, могут действовать в ней в качестве и-РНК. Помещая искусственно синтезированную информационную РНК, в состав которой входил только урацил (полиуридиловая кислота, поли-У), в бесклеточную систему, полученную из Escherichia coli, удавалось обеспечить синтез белка определенного состава. При анализе выпадающего в осадок полипептида выяснилось, что, несмотря на наличие в среде всех аминокислот, в его состав входила только одна аминокислота, а именно фениаланин, т. е. полиуридиловая кислота стимулировала синтез полифенилаланина. Тем самым была прочтена первая буква генетического кода: триплет урацил-урацил-урацил (УУУ), который контролирует включение в полипептидную цепочку аминокислоты фенилаланин.
К настоящему времени благодаря исследованиям С. Очоа, М. Ниренберга, А. Хораны и других открыты возможности расшифровки триплетов для всех аминокислот.
Используя четыре типа нуклеотидов и комбинируя их по три, можно составить 64 триплета, отличающихся друг от друга составом нуклеотидов и порядком их расположения. В настоящее время синтезированы все 64 триплета и исследована их биологическая активность, т. е. способность обеспечивать включение в белок той или иной аминокислоты. Обращает внимание то, что каждой аминокислоте соответствует несколько триплетов — кодонов, т. е. код, как принято говорить, вырожден. Кроме того, для трех из них УАГ, УАА и УГА прямыми — генетическими методами показано, что они представляют собой «нонсенсы», т. е. бессмысленные сочетания оснований, по крайней мере для бактерий и фагов.
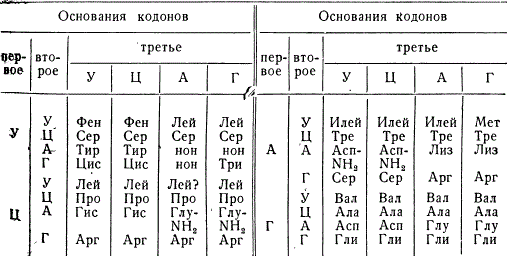
Кодоны информационной РНК, соответствующие двадцати аминокислотам
Работы по изучению кода in vitro представляют собой серьезный шаг на пути к овладению искусственным синтезом белка и тем — к более глубокому познанию тайны живой материи. Следует сказать, что триплетный код, хотя и представляется универсальным, сам есть результат эволюции под влиянием тех же факторов, которые контролируют возникновение других особенностей живых организмов.
Современные знания о функционировании гена на молекулярном уровне могут быть обобщены в следующем виде.
1. Ген характеризуется определенным набором нуклеотидов и определенной последовательностью их в ДНК.
2. В различных генах количество нуклеотидов различно.
3. Ген непосредственно не участвует в синтезе белка, с него переписывается последовательность нуклеотидов. Переписывание лишь копирует каждый участок одной нити ДНК, соответствующий более чем одному гену.
4. Первичным продуктом гена является и-PHK с последовательностью оснований, комплементарной смысловой нити ДНК; именно этот продукт гена и является детерминирующим началом для специфического белкового синтеза. При этом само считывание гена находится также под генным контролем и контролем факторов внешней среды.
5. С шаблона гена может быть скопировано много матриц и-РНК.
